
I
nduced
pluripotent
stem
cells
reprogramming
: E
pigenetics
and
applications
in
the
regenerative
medicine
R
ev
A
ssoc
M
ed
B
ras
2017; 63(2):180-189
187
the mechanisms of the aforementioned changes, optimiz-
ing their application in regenerative medicine.
R
esumo
Células-tronco de pluripotência induzida: papel da epi-
genética na reprogramação e sua aplicabilidade clínica
As células-tronco de pluripotência induzida (CTPI) ou do
inglês
induced pluripotent stem cells
(iPSCs)
são células so-
máticas reprogramadas para o estado embrionário por
meio da expressão de fatores ectópicos de transcrição
específicos, tornando-as um alvo promissor para a medi-
cina regenerativa. Apesar das CTPI compartilharem ca-
racterísticas embrionárias, como pluripotência e capaci-
dade de autorrenovação, elas possuem uma baixa
eficiência de reprogramação, sendo a memória epigené-
tica uma das principais barreiras nesse processo. A epige-
nética é caracterizada por alterações reversíveis e herdáveis
no genoma funcional que não alteram a sequência de
nucleotídeos do DNA. Dentre as diferentes modificações
epigenéticas, destacam-se metilação de DNA, alterações
em histonas e microRNA. Atualmente, sabe-se que o pro-
cesso de reprogramação efetivo das CTPI envolve um
completo remodelamento da memória epigenética somá-
tica existente, seguido pelo estabelecimento de uma “as-
sinatura epigenética” que esteja de acordo com o novo
tipo de célula a ser diferenciada. Modificações epigenéti-
cas personalizadas são capazes de melhorar o rendimen-
to e a efetividade das CTPI geradas, abrindo uma nova
perspectiva para a terapia celular. Nesta revisão reunimos
as principais informações sobre os fatores epigenéticos
que afetam a reprogramação das CTPI, bem como seus
benefícios na aplicação da terapia celular.
Palavras-chave:
células-tronco de pluripotência induzida,
medicina regenerativa, reprogramação celular, epigenética,
histonas, microRNA.
R
eferences
1.
Biehl JK, Russell B. Introduction to stem cell therapy. J Cardiovasc Nurs.
2014; 24(2):98-103; quiz 104-5.
2.
Lo B, Parham L. Ethical issues in stem cell research. Endocr Rev. 2009;
30(3):204-13.
3. Gurdon JB, Elsdale TR, Fischberg M. Sexually mature individuals of Xenopus
laevis from the transplantation of single somatic nuclei. Nature. 1958;
182(4627):64-5.
4. Tachibana M, Amato P, Sparman M, Gutierrez NM, Tippner-Hedges R, Ma
H, et al. Human embryonic stem cells derived by somatic cell nuclear transfer.
Cell. 2014; 153(6):1228-38.
5. Cowan C a, Atienza J, Melton DA, Eggan K. Nuclear reprogramming of
somatic cells after fusion with human embryonic stem cells. Science. 2005;
309(5739):1369-73.
6. Takahashi K, Yamanaka S. Induction of pluripotent stem cells frommouse
embryonic and adult fibroblast cultures by defined factors. Cell. 2006;
126(4):663-76.
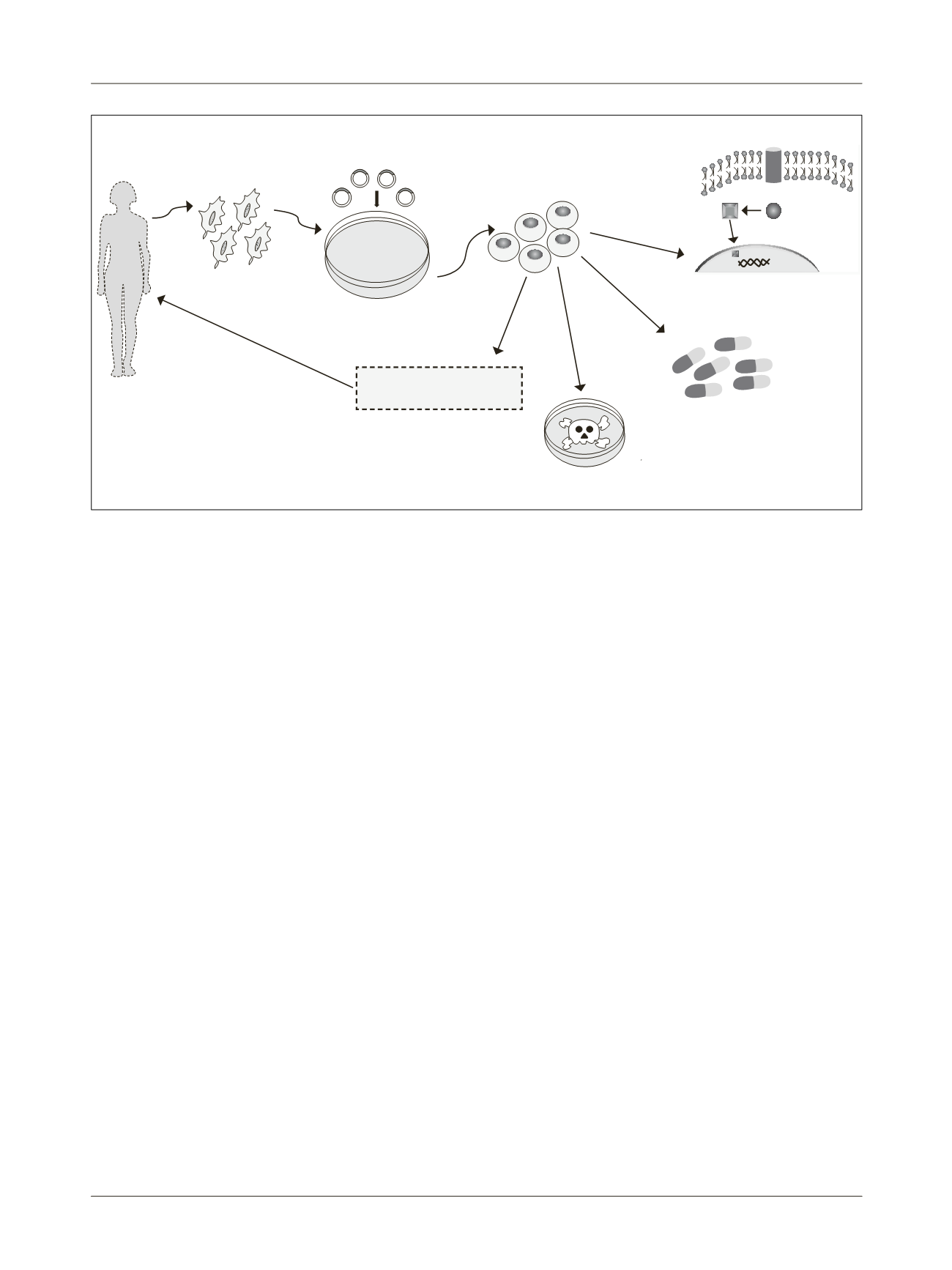
FIGURE 2
Somatic cells are reprogrammed into induced pluripotent stem cells (iPSCs). These cells are differentiated in the tissue of interest
and transplanted in an attempt to reduce the damage caused by degenerative diseases. In addition, iPSCs are also being used in pre-clinical and
clinical tests.
Fibroblasts
iPSC
Oct4
Sox2 Klf4
c-Myc
iPSC reprogramming
Toxicity test
New drugs
Pathological molecular
pathways
Differentiation in the tissue
of interest
Transplantation
















